- ŠIFRA PROJEKTA: J1-8140 (D)
- NAZIV PROJEKTA: Endokrini in genotoksični potencial inhibitorjev proteinskih kinaz: pomen za tveganja za okolje in zdravje ljudi (temeljni raziskovalni projekt)
- VODJA PROJEKTA: prof. dr. Filipič Metka (Nacionalni inštitut za biologijo)
- TRAJANJE: 1. 5. 2017 - 30. 4. 2020
- SESTAVA PROJEKTNE SKUPINE:
Nacionalni inštitut za biologijo:
doc. dr. Bojna Žegura; doc. dr. Tina Eleršek; dr. Matjaž Novak; Klara Hercog; Martina Štampar;
ONKOLOŠKI INŠTITUT LJUBLJANA:
Monika Sonc; Igor Virant; Andreja Eberl
Univerza v Ljubljani, Fakulteta za farmacijo:
prof.dr. Marija Sollner Dolenc; prof.dr. Lucija Peterlin Mašič; doc.dr. Žiga Jakopin; doc.dr. Tihomir Tomašić; dr. Martina Hrast; Maša Kenda - FTE: 1,41 FTE (skupno)
- FINANCIRANJE: Javna agencija za raziskovalno dejavnost Republike Slovenije (ARRS)
Vsebinski opis projekta
Zaskrbljenost znanstvenikov in javnosti zaradi pojava ostankov zdravil v okolju narašča, saj se je izkazalo, da so ostanki zdravil redno prisotni v zaznavnih koncentracijah v najrazličnejših hidroloških, klimatskih in talnih okoljih. Vir farmacevtskih izdelkov, ki se v vodno okolje izločajo z blatom in urinom, so iztoki bolnišnic in čistilnih naprav komunalnih odpadnih voda. Na podlagi njihovih terapevtskih lastnosti in mehanizmov delovanja, za nekatere skupine zdravil velja, da predstavljajo tveganje za ne-tarčne organizme, celo pri koncentracijah nekaj nanogramov na liter, kar še zlasti velja pri pogojih kronične izpostavljenosti [Fent in sod. 2006]. Ena takšnih skupin so protirakava zdravila. Posebno zaskrbljujoča so tista, ki izražajo genotoksično aktivnost in/ali delujejo kot hormonski motilci. Inhibitorji proteinov tirozin kinaz (TKI), so majhne molekule, ki delujejo proti specifičnim kinazam, s čimer specifično vplivajo na signalne poti, ki so deregulirane v nekaterih vrstah raka. Pri pacientih zdravljenih s TKI-ji so opazili stranske učinke, ki vključujejo spremembe v delovanju ščitnice, kostnega metabolizma, funkcije spolnih žlez, razvoju zarodka, delovanju in funkciji nadledvične žleze ter metabolizmu glukoze [Lodish, 2013], kot tudi nastanek kromosomskih sprememb v zdravih celicah (Gniot in sod., 2014) in sekundarna rakava obolenja (Kyo in sod 2012). V zadnjih 15 letih so TKI-ji postali ena izmed najpomembnejših skupin zdravil farmacevtske industrije na področju zdravljenja rakavih obolenj. V klinični uporabi je na voljo okrog 20 zdravil, ki delujejo ciljano na določene tirozinske kinaze in nekaj sto jih je v fazi kliničnih raziskav [Cohen in Alessi, 2013]. Zaradi tega njihova uporaba iz leta v leto narašča in lahko pričakujemo povečano pojavljanje ostankov teh zdravil v vodnem okolju.
Glavni cilji predlaganega projekta so:
- Raziskati porabo TKI-jev v Sloveniji in oceniti njihovo pojavljanje v okolju.
- Raziskati, ali TKI-ji, ki se trenutno uporabljajo v kliniki izražajo genotoksično in/ali endokrino aktivnost, v povezavi z njihovimi specifičnimi protein kinaznimi tarčami.
- Raziskati molekularne mehanizme genotoksične in/ali endokrine aktivnosti.
Rezultati projekta bodo dali nova znanja, katera trenutno manjkajo, so pa potrebna za ovrednotenje/ocenitev tveganja za okolje in zdravje ljudi po izpostavitvi ostankom teh zdravil.
Faze projekta in njihova realizacija
Za dosego zastavljenih ciljev, smo oblikovali načrt dela, ki je sestavljen iz šestih med seboj povezanih delovnih sklopov (DS):
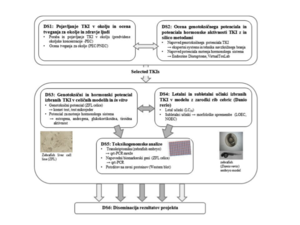
Prvi korak je izbira inhibitorjev proteinskih tirozin kinaz (TKI), ki jih bomo vključili v raziskavo (DS1), ki je osnovana na podlagi dveh kriterijev: (i) količini porabe, kjer bomo podatke pridobili iz razpoložljivih podatkovnih baz in nacionalnih poročil in (ii) razvrstitev glede na specifične tarče proteinskih tirozin kinaz. V DS2 bomo z uporabo najsodobnejših metod QSAR in navzkrižnega branja napovedali, ali izbrani TKI-ji delujejo potencialno genotoksično in kot potencialni hormonski motilci. V naslednjem koraku (DS3) bomo z uporabo in vitro testnih sistemov določali njihovo genotoksično delovanje (nastanek prelomov DNA verig in poškodbe kromosomov) in delovanje kot hormonskih motilcev (E-Screen in Callux® testi). Model zarodkov rib cebric bomo uporabili za določanje akutne toksičnosti in genotoksičnosti ter za proučevanje učinkov TKI-jev na embrionalni razvoj (DS4). Nadalje bomo na modelu zarodkov cebric s toksikogenomskimi analizami (DS5) določili profil sprememb izražanja genov po izpostavitvi TKI, kar bo omogočilo identifikacijo genov in poti, na katere vplivajo izbrani TKI-ji. Na podlagi teh podatkov, bomo opredelili specifične transkriptomske biomarkeje izpostavljenosti TKI-jem, s poudarkom na genih, ki so deregulirani zaradi genotoksične aktivnosti in zaradi motenj hormonskega delovanja. Dobljeni biomarkerji bodo ovrednoteni in potrjeni na celicah ZFL z analizo izražanja genov in proteinov. Nazadnje bomo na podlagi pridobljenih podatkov poskušali predvideti morebitne škodljive učinke proučevanih TKI-jev na ekosistem in zdravje ljudi (DS1). V celotnem obdobju trajanja projekta bo velika pozornost namenjena razširjanju rezultatov (DS6).
Realizacija v prvem letu izvajanja projekta:
V okviru DS1 je partner OI izvedel analizo porabe TKI v Sloveniji v letih 2001-2016. Ugotovili smo, da se je v Sloveniji v letih 2001 – 2005 uporabljal le imatinib, nato pa je z leti število registriranih TKI naraščalo in je danes registriranih 22. Poraba večine je tekom let naraščala, poraba nekaterih starejših, kot je imatinib, nilotinib, sorafenib pa zadnih 5 let bolj ali manj stagnira.
V okviru DS2 je partner FFA je s pomočjo orodja Endocrine Disruptome predvidel verjetnost vezave TKI na 12 različnih jedrnih receptorjev: androgen receptor, α in β estrogenska receptorja, glukokortikoidni receptor, α in β jetrna X receptorja, mineralokortikoidni receptor, peroksisomalni proliferirajoč aktiviran α, β/δ receptor, γ progesteron receptor, α retinoid X receptor ter tiroidni α in β receptor.
Na osnovi teh podatkov smo za nadaljnje raziskave izbrali 6 substanc: Imatinib, Nilotinib, Dasatinib, Sorafenib, Regorafenib in Erlotinib. Pri izbiri smo upoštevali absolutno porabo oz. trend naraščanja porabe, ter rezultate verjetnosti vezave na navedene jedrne receptorje.

