Določanje genotipa c-KIT
Uvod. Genotip gena c-KIT določamo pri bolnikih z gastrointestinalnimi stromalnimi tumorji (GIST). Mutacije v genu c-KIT so prisotne pri 80 do 90 % bolnikov z GIST-om in v manjših deležih tudi pri mieloični levkemiji, malignem timomu in melanomu. Mutacijo D816V v eksonu 17 najdemo tudi pri več kot 90 % bolnikov s sistemsko mastocitozo. Rezultati določanja genotipa gena c-KIT pri bolnikih z GIST se uporabljajo za napoved odgovora na tarčno zdravljenje z zaviralci tirozin kinaze inlahko služijo kot prognostični dejavnik (oz. pokazatelj obnašanja tumorja). Mesta mutacij v genu so različna – odvisno od vrste raka (tabela). Večina do sedaj odkritih mutacij v genu c-KIT je pri bolnikih z GIST-om v 11. eksonu (približno 70 %), nekaj jih je v eksonu 9 (od 10 do 15 %) in nekaj v eksonih 13 in 17 (od 1 do 3 %).
Tabela 1: Delež mutacij v genu c-KIT pri različnih vrstah raka.
| Vrsta raka | Delež bolnikov s prisotno mutacijo | Ekson v katerem se nahaja mutacija | |
|---|---|---|---|
| primarne mutacije | sekundarne mutacije | ||
| gastrointestinalni stromalni tumor (GIST) | 80-90 % | 9, 11, 13, 17 | 13, 14, 15, 16, 17 |
| mastocitoza | 90 % | 17 | ni podatka |
| mieloična levkemija | 15-20 % | 8, 17 | ni podatka |
| maligni timom | 7 % | 11, 14, 17 | ni podatka |
| maligni melanom | 2-6 % | 11, 13, 17, 18 | ni podatka |
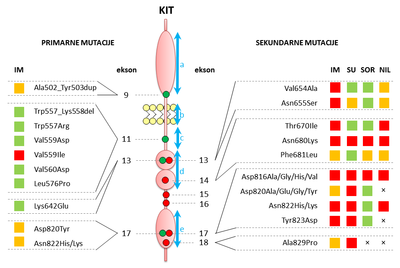
Mutacijski status gena c-KIT pri bolnikih z GIST uporabljamo kot napovedni dejavnik za odzivnost bolnika na zdravljenje z zaviralci tirozin kinaze. Za večino mutacij velja, da bodo tumorji dobro odgovorili na zdravljenje. So pa tudi izjeme, kjer je prisotnost značilnih mutacij povezana z neodzivnostjo na zdravljenje z zaviralci tirozin kinaze (slika 1). Na podlagi rezultatov analize mutacij se zdravnik odloči za vrsto zdravljenja, ki je najbolj primerna za bolnika. Med zdravljenjem z zaviralci tirozin kinaze lahko pride do nastanka sekundarnih mutacij (večinoma točkovne mutacije v eksonih 13-18), ki večinoma povzročijo neodzivnost na zdravljenje. Zato je smiselno po določenem času testiranje ponoviti. Mutacijski status gena c-KIT pri bolnikih z GIST služi tudi kot prognostični dejavnik. Glede na mesto in vrsto mutacije lahko napovemo bolj oz. manj agresivno obnašanje tumorja.
Slika 1: Struktura receptorja KIT z označenimi domenami (a, b, c, d, e) in eksoni, v katerih najdemo značilne primarne ( ) in sekundarne (
) mutacije ter odgovor tumorjev (
,
,
) s temi mutacijami na tarčna zdravila (IM, SU, SOR, NIL).
a – zunajcelična regija, b – transmembranska regija, c – povezovalna domena, d – kinazna domena 1, e – kinazna domena 2, - ni odgovora na zdravljenje,
- delni odgovor na zdravljenje,
- dober odgovor na zdravljenje, IM – imatinib, SU – sunitinib, SOR – sorafenib, NIL – nilotinib.
Vrsta vzorca. Tumorsko tkivo vklopljeno v parafin (FFPE); možno tudi sveže ali zamrznjeno tumorsko tkivo.
Metoda. Na oddelku za molekularno diagnostiko analiziramo eksone 9, 11, 13 in 17 gena c-KIT z metodo neposrednega sekvenciranja.
Čas potreben za preiskavo. 2 tedna od prejema vzorca
Reference:
- Lasota J, Miettinen M. Clinical significance of oncogenic KIT in PDGFRA mutations in gastrointestinal stromal tumors. Histopatology 2008; 53: 245-266.
- Corless CL, Schroeder A, Griffith D, Town A, McGreevey L, Harrell P, Shiraga S, Bainbridge T, Morich J, Heinrich MC. PDGFRA mutations in gastrointestinal stromal tumors: frequency, spectrum and in vitro sensitivity to imatinib. J Clin Oncol 2005; 23 (23): 5357-64.
- Beadling C, Jacobson-Dunlop E, Hodi FS, Le C, Warrick A, Patterson J, Town A, Harlow A, Cruz F 3rd, Azar S, Rubin BP, Muller S, West R, Heinrich MC, Corless CL. KIT gene mutations and copy number in melanoma subtypes. Clin Cancer Res 2008; 14 (21): 6821-8.
- Girard N. Thymic tumors: relevant molecular data in the clinic. J Thorac Oncol 2010; 5 (10 Suppl 4): S291-5.
- Ouerhani S, Gharbi H, Menif S, Safra I, Douzi K, Abbes S. KIT mutation detection in Tunisian patients with newly diagnosed myelogenous leukemia: prevalence and prognostic significance. Cancer Genet 2012; 205 (9): 436-41.
- Grgić M, Novaković S. Določanje mutacij v genih c-KIT in PDGFRA pri bolnikih z gastrointestinalnimi stromalnimi tumorji. Onkologija 2014; XVIII (1): 9-12.